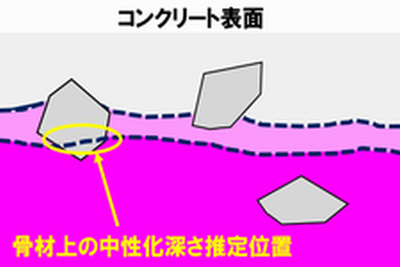
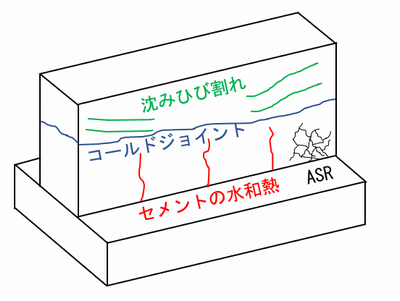
塩害とは?
塩害は、塩化物イオンCl–がコンクリート中に侵入し、アノード(陽極)と カソード(陰極)が形成され、アノード部分で鋼材の不動態被膜が破壊され腐食を生じる現象です。
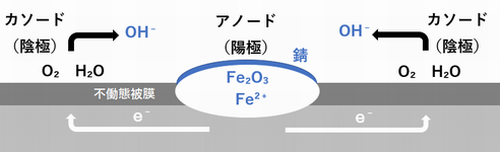
中性化も塩害も鉄筋の腐食で劣化が生じる
コンクリート構造物に、中性化や塩害を生じると、コンクリート内部の鉄筋を腐食させることで、劣化が生じます。そのため、無筋コンクリートで中性化や塩害が生じても、劣化は生じません。
中性化のメカニズム
- 大気中の二酸化炭素とコンクリート中の水酸化カルシウムが反応、炭酸カルシウムが生成
- コンクリートのpHが高アルカリ(水酸化カルシウム)から中性化(炭酸カルシウム)
- 鉄筋表面の不働態被膜が破壊(pHが下がるとさびやすくなる)
塩害のメカニズム
- 塩化物イオンがコンクリート内部に侵入
- 鉄筋表面の不動態被膜が破壊(塩化物イオンによりさびやすくなる)
※塩化物イオン=塩素イオン
塩害が生じやすい場所
塩化ナトリウム(いわゆる塩)は海水に含まれます。そのため、海岸近くでは飛来塩分により塩害が生じやすくなります。
塩化ナトリウムは、路面の凍結防止材として、塩化カルシウムは、融雪剤として広く用いられます。つまり、寒さの厳しい、内陸部の道路橋など、路面が凍結しやすい環境では、塩化ナトリウムや塩化カルシウムの散布により、塩害が生じやすくなります。
また、プールの塩素消毒で用いられるのは次亜塩素酸ナトリウム(いわゆる塩素消毒)で塩化物イオンを含むため、塩害を生じる恐れが高くなります。
鉄筋が腐食し始める塩化物イオンの量は、1.2kg/㎥とされています。
参考:土木学会コンクリート標準示方書
特徴
- 鋼材は腐食により体積が2~4倍に膨張し、膨張圧で鉄筋に沿ったひび割れを生じる
- コンクリートの水セメント比が小さいほど、セメントの水和組織が緻密となり、鉄筋腐食抵抗性が大きくなる
- 塩害を受ける環境としては乾湿を繰り返す飛沫帯が最も厳しい、次いで海上大気中、海中となる
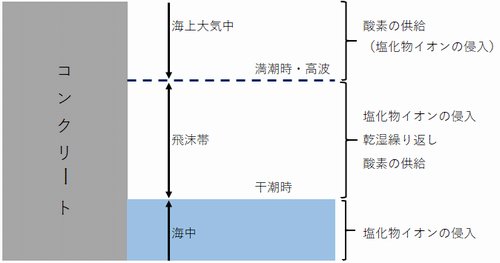
飛沫滞
塩害の化学式
コンクリート構造物に塩害が生じると、内部の鉄筋を腐食させます。この腐食反応はアソード(陽極)での酸化反応と、カソード(陰極)での還元反応により起こります。
アノード(陽極)=酸化反応
カソード(陰極)=還元反応
O2++2H2O+4e–→4OH–
腐食反応
Fe2++2OH–→Fe(OH)2+【OH–】→Fe(OH)3-【H2O】→FEOOH(赤さび)
塩化物イオンの測定
特定の位置の塩化物イオン量(濃度)を把握するために、コアからコンクリート試料を切り取る際は、乾式カッターを使用します。これは、熱による影響を避けるために水冷式のカッターを用いてしまうと、水溶性の塩化物イオンが溶出してしまうため、塩化物イオン量を精確に測定できなくなるからです。
全塩化物イオンと可溶性塩化物イオン
塩化物イオンを測定する際には、「全塩化物イオン」と「可溶性塩化物イオン」を意識して測定する必要があります。
全塩化物イオン
- 硬化コンクリート中に含まれる全ての塩化物イオン
- 微粉末(150μm以下)にしたコンクリート試料を用いる
- 強酸(硝酸等)を加えて、30分撹拌し、コンクリートをほぼ完全に分解した後、加熱煮沸し抽出する
- 固定化されたフリーデル氏塩も強酸により分解され、塩化物イオンが溶出される(一般に、フリーデル氏塩はセメント量の0.4%程度が固定化されると言われています。)
可溶性塩化物イオン
- コンクリートの水中を動きやすい塩化物
- 鋼材の腐食に影響する
- 資料を50℃に温め、50℃の温水で30分間振とうした後、保温・静置してろ液を採取する
硬化コンクリート中の塩化物イオン量の測定方法
重量法
- 例:塩化銀沈殿法
- 塩化物イオンと銀イオンを反応させて、塩化銀(沈殿物)を生じさせてその重量を測定する
- Ag++Cl–=AgCl
容積法
- 例:モール法
- クロム酸カリウム(クロム酸イオン)を指示薬とし、塩化物イオン濃度が不明な水溶液に硝酸銀水溶液を加える
- 塩化物イオンが先に塩化銀として沈殿し完全に反応が終わると、クロム酸銀が生じ、溶液が赤褐色に呈色する
- 溶液が呈色した時点の、加えた硝酸銀水溶液の容積(体積)から塩化物イオンの量を測定する
吸光光度法
- 例:クロム酸銀法
- 塩化物イオンを含む水溶液にクロム酸銀を加える
- 塩化物イオンが塩化銀として生成し、クロム酸イオンが遊離生成される
- クロム酸イオンの吸光度(光を吸収する程度)を測定して、塩化物イオンの量を測定する
電気化学的方法
- 例:電位差滴定法
- 塩化物イオンを含む溶液に電極を設置し、電位差(単位:ボルト)を測定する
- 塩化物イオンを含む溶液に硝酸銀溶液を滴定する(滴定:濃度がわかる溶液を少しずつ加えること)
- 硝酸銀溶液の滴定量と電位差の変化から塩化物イオンの量を測定する(JIS A 1154)