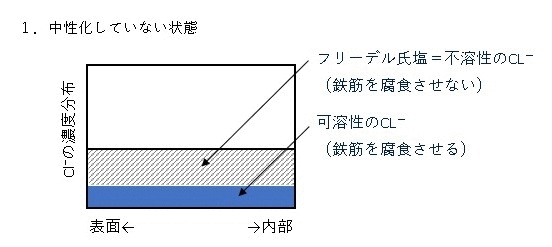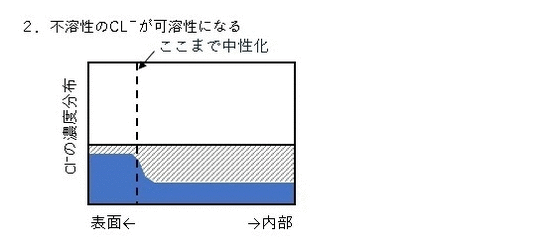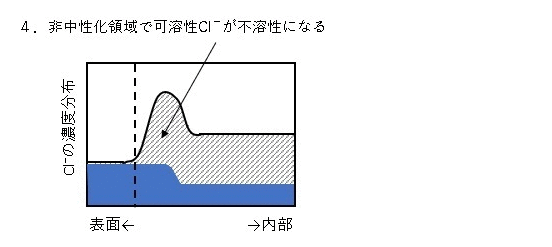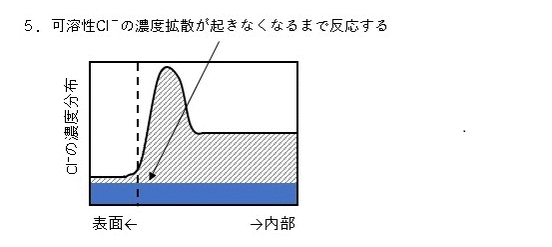
コンクリート診断士過去問2003-No.22
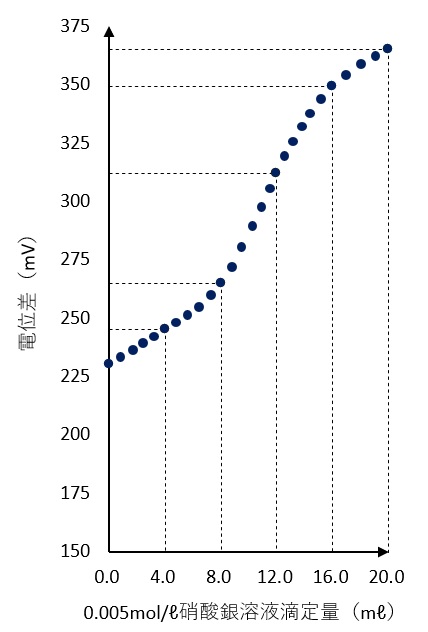
コンクリートの微粉末5g中の全塩化物イオンを溶解させた溶液において、電位差滴定法を用いて全塩化物イオン量を測定することとし、下図を得た。コンクリートの密度をg/cm3、使用したmol/l硝酸銀溶液1mlの塩化物イオン相当量を0.000178gとするとき、コンクリート中の全塩化物イオン量として最も近い値はどれか。
なお、空実験として行ったコンクリート微粉末試料を用いない溶液の硝酸銀溶液滴定量は2.0ml、使用した硝酸銀溶液のファクターは1.000であった。
(1)0.5kg/m3
(2)0.8kg/m3
(3)1.1kg/m3
(4)1.5kg/m3
まずは、molとは何か?
この問題では、molを使用する必要はありませんが、高校化学の復習だと思ってください。
1mol=6.02×1023個
(1ダース=12個みたいなものと思ってください。)
求めるものは?=微粉末5g中に含まれる全塩化物イオンの量
硝酸銀水溶液を用いた滴定法の化学式
Ag++Cl–→AgCl
ここで、AgCl(塩化銀)は沈殿物として溶液中に生成されます。
問題より、滴定に用いる硝酸銀溶液1mlに含まれる塩化物イオンの量は0.000178g/mlであることが読み取れます。
反曲点が表れる点は、溶液中の塩化物イオンがすべて反応したことを表します。
この問題では、12.0mlの滴定量で反曲点を迎えていることから、溶液中の塩化物イオン量は下の式で表すことが出来ます。
試料5g中に含まれる塩化物イオン量=(滴定量-空試験)×塩化物イオン相当量×ファクター
=(12.0-2.0)ml×0.000178g/ml×1.00
=0.00178g
つまり、コンクリート5g中には0.00178gの塩化物イオンが含まれていることになります。
これを、コンクリート中の全塩化物量(kg/m3)にするには、まず、5gのコンクリートの容積を求めます。
容積×密度=重量 より
容積=重量/密度 の関係が分かります。
重量=5g、密度=2.3g/cm3より
5g/2.30g/cm3=2.1739cm3
先ほどのコンクリート5g中に含まれている塩化物イオンの量は0.00178gなので
コンクリート5gの容積は2.1739cm3との関係から
0.00178g/2.1739cm3=0.0008g/cm3
単位を揃えると
0.0008g/cm3=0.8kg/m3
答えは(3)になります。
以上、過去問の解答例でした。参考にしてください。